RNA干擾(RNAi)是許多真核生物中一種保守的RNA沉默機制, 小干擾RNA是RNA干擾的關鍵組成部分。在小RNA的加工過程中,Dicer家族蛋白起到了重要的作用,它們發揮作用的過程中常需要雙鏈結合蛋白(dsRBP)作為輔因子來幫助它們發揮功能。在果蠅中,siRNA的產生是由ATP依賴型的Dicer-2(Dcr-2)蛋白在其輔因子Loqs-PD的輔助下,從長的雙鏈RNA(dsRNA)上等距切割產生21個堿基對的雙鏈siRNA。但是對于ATP依賴型的Dicer-2蛋白如何識別并切割RNA底物整個過程的分子機制仍不清楚。
2022年7月14日,清華大學生命科學學院王宏偉課題組與復旦大學麻錦彪課題組合作,在《自然》(Nature)雜志上發表了題為“果蠅Dicer-2/Loqs-PD處理雙鏈RNA的結構機制”(Structural insights into dsRNA processing by Drosophila Dicer-2–Loqs-PD)的研究論文,通過冷凍電鏡單顆粒技術解析了包括Dicer-2/Loqs-PD以及dsRNA的6個不同狀態冷凍電鏡結構(圖1),并結合生化分析首次揭示了Dicer-2/Loqs-PD復合物結合并切割雙鏈RNA產生siRNA的分子機制。
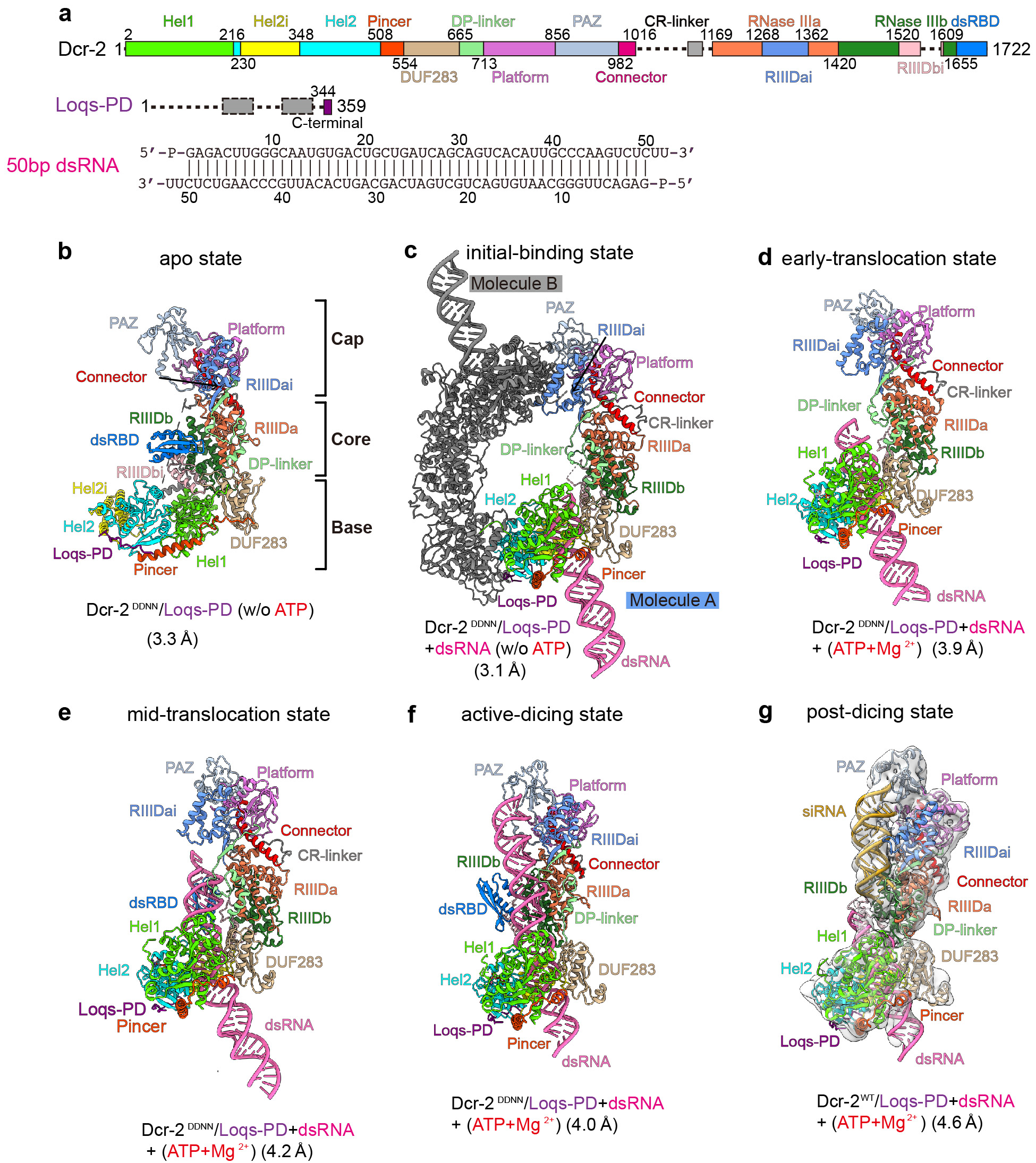
圖1,Dicer-2/Loqs-PD復合物結構域示意圖,以及結合雙鏈RNA加工生成siRNA過程不同狀態的冷凍電鏡結構。
研究團隊從活性位點突變的Dicer-2/Loqs-PD單獨蛋白(apo)復合物結構開始解析。之后加入了雙鏈RNA,獲得了無ATP時,處在初始結合狀態的Dicer-2/Loqs-PD–dsRNA復合物高分辨結構。發現在apo狀態下松散的解旋酶結構域在初始結合狀態中像手一樣包裹住了雙鏈RNA并扭曲了RNA的軸,此時解旋酶中的Hel1與Hel2亞結構域組成了成熟的ATP結合位點。在該狀態下還明確了Loqs-PD主要通過C端與Dicer-2的解旋酶區域緊密結合的分子機制。在初始狀態的基礎上,進一步加入ATP和鎂離子,通過數據收集與計算分類,得到了切割活性狀態與兩種明顯具有不同結構特點的移位狀態;與初始狀態比較,兩種移位狀態中的Dicer-2–Loqs-PD復合物分別在雙鏈RNA上移動了8bp和17bp左右,其中早期移位狀態(~8bp)可以看作是在初始狀態上的延伸,而中期移位狀態(~17bp)中由于雙鏈RNA穿過解旋酶的長度足夠長,使得Dicer-2 C端的dsRBD結構域能夠結合雙鏈RNA,并對RNA的軸進行了進一步的偏轉,使其指向能夠識別末端PAZ-Platform結構域,RNA進一步的深入會使得其末端結合到PAZ-Platform結構域。之后,隨著ATP水解導致的RNA進一步的深入、形變,從而產生的力使得解旋酶結構域以外的區域(cap-core區域)作為一個整體被RNA撐開,RNA進一步深入,最終到達切割活性狀態,cap-core區域則緊密的結合在雙鏈RNA上,確保精確的21bp siRNA的生成。之后研究者們使用正常活性的Dicer-2蛋白,獲得了處于切割后狀態的復合物,并通過分析發現它處于完成切割后正在回復到的早起移位狀態的過程中。從而將整個過程串起,闡明了Dicer-2–Loqs-PD復合物從結合雙鏈RNA并在其上移動,到形成切割活性狀態,直至切割完成產生siRNA的整個循環過程的分子機制和其中連續且遞進的構象變化。
清華大學生命學院王宏偉教授、復旦大學麻錦彪教授為論文共同通訊作者,復旦大學蘇世晨博士和清華大學王家博士為論文共同第一作者,清華大學劉楠博士、李曉敏博士為樣品制備和數據收集提供了重大幫助。國家蛋白質科學中心(北京)、清華大學冷凍電鏡平臺、清華大學高性能計算平臺和水木未來(北京)科技有限公司為本研究提供了設備和技術支持。本研究得到了國家自然科學基金、國家重點研發計劃、北京結構生物學高精尖創新中心、清華-北大生命科學聯合中心以及Xplorer獎項等經費的支持。