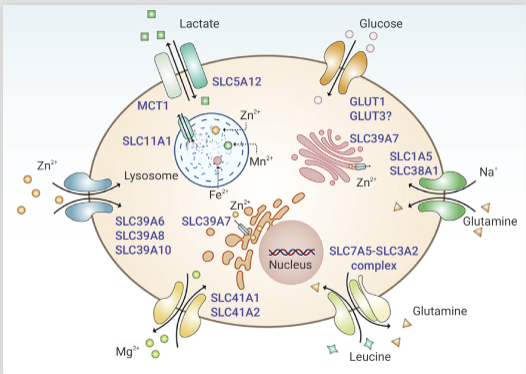
關于細胞的程序性死亡的相關研究一直是生命科學的熱門領域,無論是持續火熱的"鐵死亡" (推文:鐵死亡是什么,如何檢測?您要的 “一文通” 來了)。還是正在生信領域大方異彩的 “銅死亡” (推文:空降 "熱搜" 銅死亡丨解鎖細胞死亡新方式),都涉及到 "離子轉運"。在轉運過程中,溶質載體 (Solute Carriers, SLC) 轉運蛋白家族作為重要的膜轉運蛋白家族,它們對葡萄糖、氨基酸和金屬離子的轉運有著重要的影響 (圖 1)
圖 1. SLC 蛋白家族對不同離子以及氨基酸等轉運
SLC7A11----死亡調控途徑中的雙刃劍
SLC 家族成員 SLC7A11 轉運蛋白在維持細胞內谷胱甘肽水平和保護細胞免受氧化應激誘導的細胞死亡方面具有重要作用,具有公認的促生存作用。但有研究表明,膠質母細胞瘤細胞在葡萄糖剝奪條件下,通過 System Xc- (其中 SLC7A11 為催化亞基) 攝取胱氨酸會迅速誘導 NADPH 耗竭、活性氧物質積累和細胞死亡。
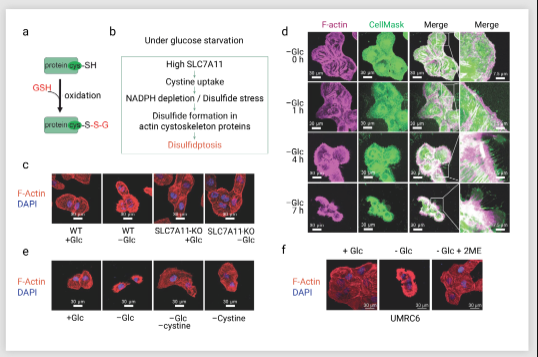
2020 年甘波誼團隊在 Nature Cell Biology 發表的文章也表明,葡萄糖饑餓條件下,高 SLC7A11表達反而促進細胞死亡,SLC7A11 就像是調節細胞氧化還原平衡和細胞死亡/存活方面的雙刃劍。
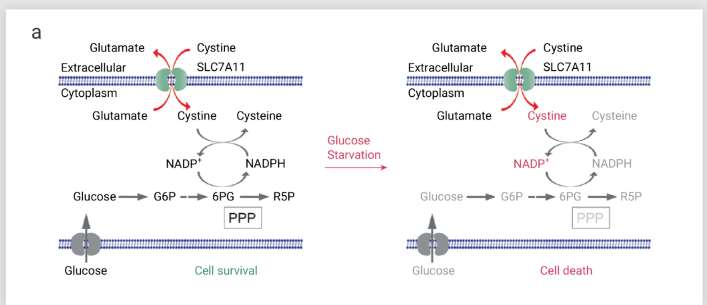
圖 2. 葡萄糖饑餓條件下,高 SLC7A11 表達反而促進細胞死亡
SLC7A11 和 SLC3A2 組成的胱氨酸/谷氨酸逆向轉運蛋白 System Xc -,將胞內谷氨酸轉出以 1:1 的比例來換取胞外的胱氨酸 (Cys2)
■ SLC7A11 高表達為何會 “促” 死亡?
這是因為胱氨酸是種不溶性氨基酸,為了防止細胞內高度不溶性胱氨酸的毒性積聚,SLC7A11high細胞需要迅速將胱氨酸還原為半胱氨酸,而這個過程需要從葡萄糖-戊糖磷酸途徑(PPP)獲得大量NADPH,這會對細胞NADPH 庫會造成大量消耗,并使此類細胞產生葡萄糖和戊糖磷酸途徑(PPP)依賴性(如圖 2)。因此, 當葡萄糖供應限制,氧化還原力不足,SLC7A11high 細胞內的胱氨酸或其他二硫化物分子的異常積累,誘發二硫化物應激觸發細胞死亡。
今年2月,甘波誼團隊發表的 Actin cytoskeleton vulnerability to disulfide stress mediates disulfidptosis 一文更加詳細闡明了這一死亡機制,研究表明肌動蛋白細胞骨架對二硫化應激的敏感性介導了雙硫死亡 (disulfidptosis),并提出了在癌癥治療中靶向二硫化的治療策略。
SLC7A11-high 細胞的獨特細胞死亡方式
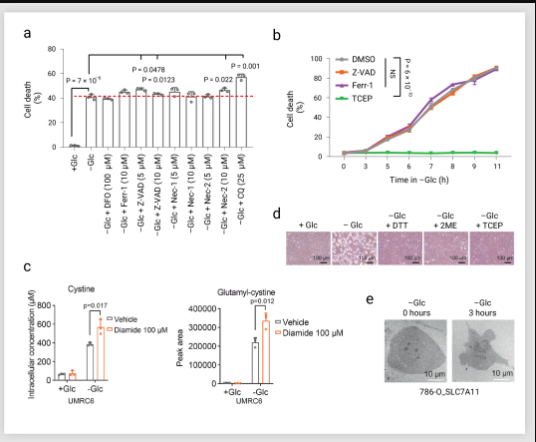
雙硫死亡是一種不同于鐵死亡,凋亡等的新型死亡方式,在 SLC7A11high 細胞中,鐵死亡,凋亡,細胞壞死以及自噬抑制劑都不能挽救葡萄糖饑餓誘導的細胞死亡 (圖 3a-b), 但二硫應激的還原劑,如二硫蘇糖醇 (DTT)、β-巰基乙醇 (2ME) 和 TCEP 可以完全抑制 SLC7A11high 細胞中葡萄糖饑餓誘導的細胞死亡 (圖 3d)。此外,硫醇氧化劑(二胺和馬來酸二乙酯)促進 SLC7A11high細胞在葡萄糖饑餓下的細胞死亡,并導致細胞內二硫分子的急劇積累(如胱氨酸和谷氨酰胱氨酸,經二胺處理后進一步增加) (圖 3c)。透射電鏡分析顯示,在葡萄糖饑餓導致 SLC7A11high 細胞種胱氨酸在細胞質中積聚 (圖 3e)。以上結果表明二硫脅迫引起的細胞死亡,與鐵死亡,細胞凋亡等都不同,那么其特征到底是什么?
圖 3. 葡萄糖饑餓條件下的細胞死亡方式
雙硫死亡---與肌動蛋白細胞骨架有關
作者團隊假設,在葡萄糖饑餓條件下,SLC7A11 高細胞的 NADPH 消耗和二硫應激的增加誘導氧化還原敏感蛋白中二硫鍵的生成 (在正常條件下,細胞質的還原環境阻止胞質蛋白形成二硫鍵),這可能會破壞相應的氧化蛋白的活性或功能,從而損害細胞活力。
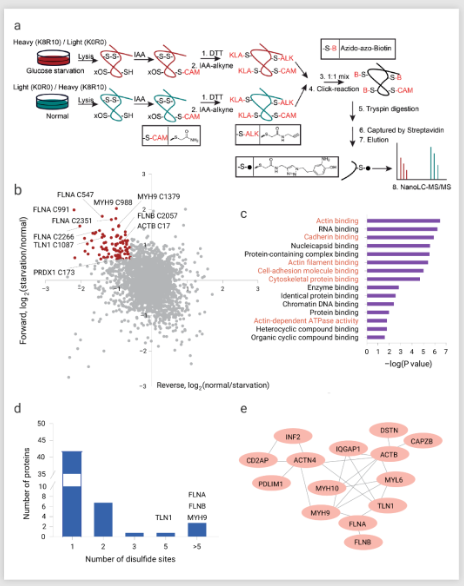
為了驗證這一假設,作者團隊對氨基酸進行穩定同位素標記 ,量化葡萄糖饑餓誘導的SLC7A11high 細胞中的二硫化物蛋白質組改變 (圖 4a)。正向和反向標記分析確定了 90 個半胱氨酸位點。此外,基因本體分析表明,在葡萄糖饑餓誘導的二硫鍵的蛋白質中,肌動蛋白細胞骨架和細胞粘附相關的生物過程或途徑顯著富集 (圖 4c),作者團隊還發現了至少 17 個肌動蛋白細胞骨架蛋白在葡萄糖饑餓后二硫鍵增加的頂級蛋白中 (圖 4b) 并且這些蛋白質中的大多數包含二硫鍵的半胱氨酸位點 (圖 4d-e)。這表明 SLC7A11high 細胞中的葡萄糖饑餓可能誘導肌動蛋白細胞骨架蛋白中的二硫鍵 (圖 4c)。
圖 4. 葡萄糖饑餓條件下肌動蛋白細胞骨架蛋白中的二硫鍵形成
SLC7A11-high 細胞的肌動蛋白細胞骨架動力學
由于二硫鍵的形成會影響非還原條件下蛋白質的電泳遷移率。作者團隊檢測了肌動蛋白細胞骨架蛋白的遷移率,發現 UMRC6 細胞在葡萄糖饑餓后,多個肌動蛋白細胞骨架蛋白表現出較慢的遷移,這表明這些肌動蛋白細胞骨架蛋白在葡萄糖饑餓條件下形成多個分子間二硫鍵 (圖 5a),
作者團隊還進一步研究葡萄糖饑餓后 SLC7A11high 細胞的肌動蛋白細胞骨架動力學。在含糖培養基的 SLC7A11high 細胞中,肌動蛋白絲 (F-肌動蛋白) 主要在細胞皮質和應激纖維中;但葡萄糖饑餓會誘導細胞形態的顯著變化:細胞收縮和 F-肌動蛋白收縮。F-actin 與膜染料 CellMask 共染色顯示,葡萄糖饑餓會導致 SLC7A11high 細胞中 F-肌動蛋白從質膜分離(圖 5b-d),并且葡萄糖饑餓誘導的這些細胞肌動蛋白細胞骨架形態的變化是 SLC7A11依賴性的( 圖 5c) ,胱氨酸饑餓 、2DG 或 2ME (圖 5f) 處理可以消除這種變化。葡萄糖饑餓誘導的 SLC7A11 高細胞肌動蛋白骨架蛋白異常二硫鍵可能導致隨后的 F-肌動蛋白收縮和脫離質膜。
圖 5. 葡萄糖饑餓條件下,異常二硫鍵形成導致的肌動蛋白動力學
以上結果表明,SLC7A11high 細胞中,葡萄糖饑餓誘導肌動蛋白細胞骨架蛋白的異常二硫鍵,F-肌動蛋白以 SLC7A11 依賴性的方式崩潰。新的死亡機制的鑒定促進人們對細胞穩態的基本理解,那 “雙硫死亡” 最大的意義何在?
雙硫死亡,研究的意義何在?
葡萄糖是糖酵解的起始物質,由葡萄糖轉運蛋白 (GLUT) 家族通過細胞膜轉運,靶向葡萄糖轉運蛋白(GLUT) 是是潛在癌癥治療干預的有趣靶點。
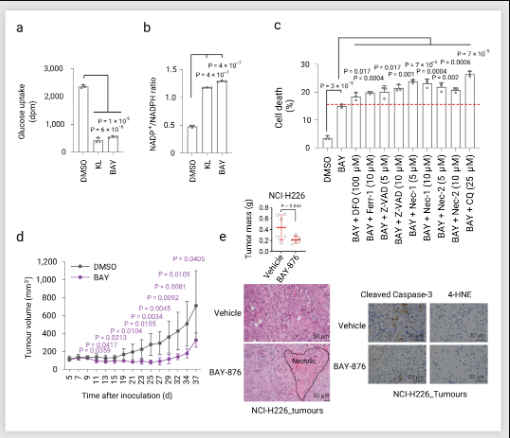
甘波誼團隊等人在 2020 年的發表的文章中就發現高 SLC7A11 表達的癌細胞對葡萄糖轉運蛋白GLUT 抑制劑特別敏感。GLUT 抑制劑 KL-11743 或 Bay-876 可有效抑制葡萄糖攝取,與葡萄糖饑餓情況相似。在 SLC7A11 過表達細胞中,GLUT1 抑制劑處理增加 NADP+/NADPH比值 (圖6a,b),并在 UMRC6 細胞中引發強烈的細胞死亡(圖 6c)。此外,GLUT 抑制會誘導二硫鍵的結合肌動蛋白骨架蛋白和 F-肌動蛋白網絡崩潰。
在動物模型中,Bay876 治療降低了 SLC7A11high NCI-H226異種移植瘤的生長 (圖 6d),Bay-876 處理的腫瘤表現出頻繁的細胞死亡 (圖 6e),Bay-876 處理的腫瘤在肌動蛋白細胞骨架蛋白中表現出更多的二硫鍵結合。這些結果表明:GLUT 抑制劑誘導 SLC7A11high 癌細胞的雙硫狀態和細胞死亡,而癌細胞的雙硫死亡可能是介導 GLUT 抑制劑治療 SLC7A11high 腫瘤的治療效果的關鍵因素。
圖 6. GLUT 抑制劑誘導 SLC7A11 高表達細胞死亡
■ 小結
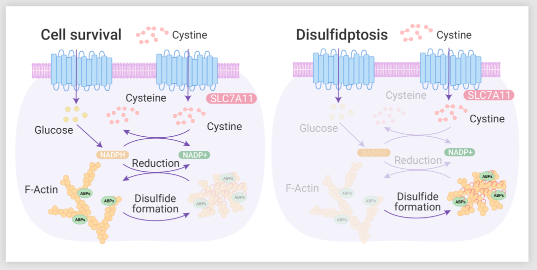
作者團隊研究結果表明在 SLC7A11 高表達的情況下,葡萄糖饑餓限制 PPP 產生 NADPH 會導致小分子二硫化物 (包括胱氨酸) 大量積累、引起一系列氧化還原缺陷和細胞死亡。
圖 7. 雙硫死亡的機制圖
并且基于對雙硫死亡的機制理解,還發現 GLUT 抑制誘導的雙硫死亡可能是治療slc7a11 高表達腫瘤的有效治療策略,這種腫瘤經常發生在人類癌癥中。雙硫死亡這種獨特的細胞死亡機制的闡明為靶向治療癌癥提供一個關鍵框架。
相關產品
一種有效的能透過血腦屏障的壞死性凋亡 (necroptosis) 抑制劑,Necrostatin-1 (Nec-1) 也是一種 (IDO) 抑制劑。
RSL3 ((1S,3R)-RSL3)
谷胱甘肽過氧化物酶 4 (GPX4) 的抑制劑 (ferroptosis 激動劑),可降低 GPX4 的表達
有效的、選擇性的 ferroptosis 抑制劑。Ferrostatin-1 是一種人工合成的抗氧化劑,通過還原機制來防止膜脂的損傷,從而抑制細胞死亡。具有抗真菌活性。
Chloroquine
Chloroquine 是自噬 (autophagy) 和 Toll 樣受體 (TLRs) 的抑制劑。Chloroquine 有效抑制 SARS-CoV-2 (COVID-19) 感染 (EC50=1.13 μM)。
Deferoxamine (Deferoxamine B)
鐵螯合劑 (結合 Fe(III) 和許多其他金屬陽離子),被廣泛用于減少鐵在組織中的積累和沉積。
凋亡誘導劑。是一種有效,ATP 競爭性的,非選擇性蛋白激酶抑制劑
2-Deoxy-D-glucose
葡萄糖類似物,為葡萄糖代謝抑制劑,通過作用于己糖激酶 (hexokinase) 來抑制糖酵解 (glycolysis)。
BAY-876
一種具有口服活性的,選擇性的葡萄糖轉運蛋白 1 (GLUT1) 抑制劑,IC50 為 2 nM。BAY-876 對 GLUT1 的選擇性是 GLUT2,GLUT3 和 GLUT4 的 130 倍以上。
KL-11743
具有口服活性的葡萄糖競爭性 I 類葡萄糖轉運蛋白抑制劑,抑制 GLUT1,GLUT2,GLUT3 和 GLUT4 的 IC50 值分別為 115 nM,137 nM,90 nM 和 68 nM。KL-11743 特異性阻斷葡萄糖代謝。KL-11743 可與電子傳遞抑制劑協同誘導細胞死亡。