MS/MS操作模式
串聯質譜儀通常使用的都是離子模式來鑒定蛋白質的氨基酸序列。目前所有的MS/MS質譜儀都具有該功能。不過其它特殊的質譜儀也具有MS/MS功能。如果要發現蛋白質中的某個功能基團則需要用到母離子掃描功能或者中性丟失掃描功能,而這就必須用到三重四級桿質譜儀,如Q-Q-Q質譜儀,或四級桿離子阱質譜儀,如Q-Q-LIT質譜儀。比如復雜混合物里的蛋白質磷酸化位點和糖基化位點就都可以用這種方法(在碰撞池中產生特殊的報告離子,通過它來進行特殊的功能檢測)檢測出來。在一個典型的質譜檢測試驗中,首先先用母離子掃描或中性丟失掃描都能發現目標組分,然后再用傳統的MS/MS方法鑒定蛋白質的氨基酸序列以及定位修飾位點。
三重四級桿質譜儀在MRM模式下也能以極高的敏感度進行定量分析。已知的或未知的分析物都以極高的敏感度和選擇性能被定量檢測出來。這種高選擇性得益于質譜儀能夠對代表一個肽段的一對母離子和片段裂解物離子進行實時監測。而且,在MRM模式下進行的兩輪選擇過程會極大地提高檢測的靈敏度,因為第一輪篩選過后只能剩下很少的離子,這也就將背景噪聲減小到了最低水平。碰撞誘導解離片段離子(collision-induced dissociation fragment ions, CID)來源于母離子,這些CID離子能夠產生離散信號,而背景化學噪聲信號則是隨機分布的。最后,由于這種采樣時間很長的技術固有的非掃描本質使得它的敏感度非常高,相比離子掃描技術的探測極限(LOD)要高出好幾個數量級。
質譜儀的性能
總體來說,質譜儀的性能包括分辨率、敏感度或探測極限和準確性等,這些性能都與質譜儀的類型、采用的離子化方法和掃描能力有關。不過沒有哪一個儀器能同時在上述所有方面都全面占優,在選擇儀器的時候必須根據實驗需要進行相應的取舍。
對實驗儀器性能的比較一直以來都是一個存在很多爭議的話題。因為性能是服務于需求的,是取決于待測樣品和實驗步驟的。質譜儀對單獨肽段樣品進行檢測時敏感度總是很低,不過如果生物樣品的基質背景(matrix background)很高,那么檢測的敏感度就會提高好幾個數量級。這種同一款儀器在性能上表現出來的“不穩定性”其實很常見,在儀器處于不同操作條件或狀態下時(比如在最優條件下,常規條件下和大批量處理條件下)它們的性能表現都是不同的。實驗目的是想進行定量分析還是蛋白質鑒定,這也決定了該使用哪種儀器。在蛋白質鑒定試驗中,儀器的分辨率(能很好地區分不同組分)和準確性是最主要的,而在定量研究中,敏感度、動態范圍和MRM能力才是最主要的。因此,我們應該根據實驗目的的需要以及實驗設計安排來確定該使用哪種質譜儀。
要想用全掃描模式(full scanmode)獲取定量數據的同時再用MS/MS模式獲取定性數據是一件非常困難的事情。不過某些“雜交”質譜儀,比如LIT-ICR質譜儀,由于它們能夠平行采集數據,因此可以部分解決上面那個問題。精確的定量分析需要源自整個洗脫圖(entire elution profile)的高質量的、高信噪比的數據信息。數據質量與數據采集參數高度相關,這些數據采集參數包括掃描時間或者采樣時間(對于非掃描質譜儀而言)。因此,我們經常需要在數據質量和樣品處理能力(量)之間做出取舍。
最新進展
最近又有幾項有關質譜儀的最新進展問世,這些新成果的出現又給我們的生物大分子研究工作補充了“彈藥”。在蛋白質測序方面,基于碰撞誘導裂解技術(CID),又新出現了可變裂解技術(Alternate fragmentation technique),該新技術是基于處在碰撞池中的離子具有的電子傳遞特性開發出來的。目前,電子捕獲解離技術(ECD)和電子傳遞解離技術(ETD)都已經分別被應用到FT-ICR質譜儀和LIT質譜儀上了。運用這兩種技術產生的蛋白質裂解產物能與經典的CID方法裂解產物互為補充。不過這兩種新方法裂解更均勻,更適合用于發現翻譯后修飾情況。ECD技術和ETD技術還都可以用于大型肽段和蛋白質的研究。他們的裂解能力和對完整蛋白的分析能力可以幫助我們直接用質譜儀對完整的蛋白質進行分析,即可以采用所謂的“自上而下(top-down)”的方法進行研究。這樣,我們能夠獲得完整的氨基酸序列信息和翻譯后修飾信息,能夠對蛋白質進行最準確的鑒定。
傳統的和最新的蛋白質組學研究策略
雖然到目前為止,還沒有一種蛋白質組學研究策略能夠對某個蛋白質組進行常規的、完整的分析,但是現在的技術已經非常強大,我們相信,很快就能進行全蛋白質組學研究了。而且,對某個亞蛋白質組(比如某個細胞器或亞細胞結構的蛋白質組)進行研究早就已經不是什么難題了,這已經成為了一種常規的研究手段。不過,蛋白質組學研究方法也需要視研究目的而做出相應的調整,不能千篇一律。比如有很多研究都是描述性的研究項目,主要的關注點都著眼在發現、鑒定出蛋白質以及這些蛋白質的翻譯后修飾情況,而最近又開始逐漸興起蛋白質組學定量研究了。
實際上,每一個以質譜檢測為基礎的蛋白質組學研究工作都包括以下3大部分:(i)分離、消化蛋白質樣品,然后對樣品進行進一步裂解;(ii)對樣品進行質譜定性和定量檢測;(iii)用相應的軟件對質譜檢測結果進行分析處理,獲得蛋白質的氨基酸序列,并且如果可能的話,進行定量分析。蛋白質的鑒定工作主要由MS/MS質譜儀負責,然后通過將質譜檢測結果與數據庫中的數據進行比對,最后確定出蛋白質的氨基酸序列。需要提醒的是,對結果的統計分析工作是保證結果正確性的關鍵。
對純化蛋白進行質譜分析
下面,我們用最“古老”的蛋白質組學研究方法——2維凝膠電泳法(two-dimensional gel electrophoresis, 2DE)結合質譜分析法對純化蛋白進行質譜分析的策略為例進行介紹(圖2A)。首先,待測目標蛋白經消化、酶解之后經由質譜儀進行鑒定,通常使用的都是MALDI-ToF質譜儀來獲取肽鏈指紋圖譜(peptide mass fingerprint)。最近,出現了好幾種該策略的改進方法,即將各種連續電泳分離方法(sequential electrophoretic separation method)或色譜分離方法(chromatographic separation method)結合進來,以提高質譜檢測時的峰容量,這樣就提高了對復雜樣品的分辨率。定量分析則是在蛋白質水平通過比較不同樣品中目標蛋白的信號強度來完成的。這種策略的優劣取決于它們區分相關(近)蛋白質的能力,即分辨率的高低,比如要能夠區分出經不同類型修飾的蛋白質,還取決于待測樣品的復雜程度。這種研究策略最大的問題是動態范圍太窄,而且處理樣品的能力也不夠高,不具備高通量分析的功能,因此不足以進行蛋白質組學研究。而且,一些比較重要的蛋白質,比如膜蛋白等還不能用該方法進行分析,因為該方法只能用于分析復雜度比較低的樣品,或者用于對某一特定蛋白進行分析的實驗。
對復雜樣品進行質譜檢測
對復雜樣品進行質譜檢測時也用到了人類基因組研究項目中用到的“鳥槍法”策略。即首先將蛋白質組樣品進行裂解,這樣獲得的多肽片段才能夠用于自動化MS/MS分析,我們常用的是快速掃描設備如IT質譜儀(圖2B)。用這種方法可以對完整細胞裂解物或組織提取物進行分析,也可以對亞細胞結構、提純的細胞器或其它亞蛋白質組樣品進行檢測。
如果給待測樣品帶上穩定的同位素標記,我們就可以對樣品中不同蛋白質的豐度進行檢測了,這些蛋白質可能在化學性質方面是一樣的,但是我們可以通過不同的同位素信號強度比對它們進行區分(圖3A)。也可以使用如圖3B中所示的串聯標記(tandem mass tag)方法對樣品進行多次質譜分析。還可以在進行質譜分析之前往待測樣品中添加定量的同位素標記肽段,以獲得樣品準確的定量數據(圖3C)。
這種“鳥槍法”最大的優勢就是簡單,不論從理論層面來說還是從實驗操作層面來說都很簡單,該方法相比前面所述的各種方法能夠對蛋白質組分進行更大程度的覆蓋,同時定量的準確性更高。不過該方法也有其局限性,具體表現在動態范圍不夠,難以使用生物信息學方法從大量的、高冗余的、復雜的蛋白質組樣品質譜數據中推斷出蛋白質序列。幸好這些問題已經部分得到了解決,通過裂解的方法可以降低樣品的復雜程度。常用的裂解方法主要針對的都是蛋白質組中生物信息學資料豐富的部分,比如富含半胱氨酸的肽段、磷酸化的肽段、糖基化的肽段等等。這種“鳥槍法”策略最適合用于快速鑒定復雜樣品中的組分,也非常適合用于對不同樣品中同一蛋白質的定量比較研究。在“鳥槍法”策略中,在蛋白質水解過程里,不同肽段間的聯系信息以及肽段與其來源蛋白質間的聯系信息都已經丟失了,因此該方法不太適合用于對具有多重修飾的蛋白質進行鑒定工作。
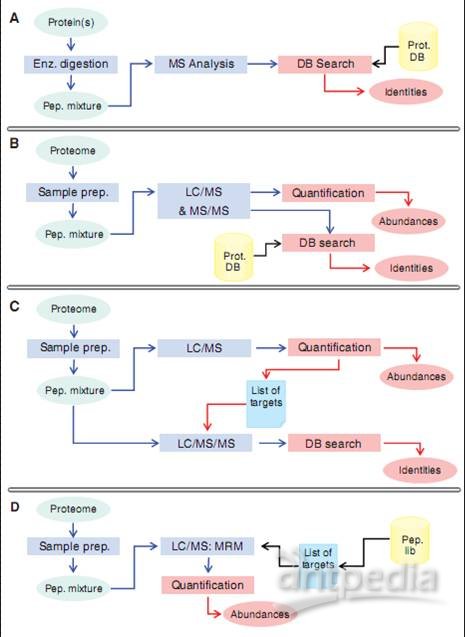
蛋白質組學研究策略示意圖
Protein(s):待測蛋白質樣品;Enz. Digestion:酶解;Pep. Mixture:裂解產物混合物;
MS Analysis:質譜檢測分析;DB Search:數據庫比對搜索;Identities:鑒定;
Prot.DB :蛋白質數據庫;Proteome:蛋白質組;Sample prep:樣品準備(裂解);
LC/MS& MS/MS:LC/MS以及 MS/MS分析;Quantification:定量研究;
Abundances:豐度;List of targets:挑選出待測樣品;Pep.lib:待測靶樣品;
圖2 蛋白質組學研究策略示意圖。A:經由2維電泳或pull-down實驗發現的待測蛋白質樣品prot隨即被酶解,然后用質譜儀對酶解片段pep進行質譜檢測分析。最后根據肽質指紋圖譜(PMF)鑒定出肽段以及它們的來源蛋白。其它的MS/MS數據也能用來進行肽段鑒定。B:隨機蛋白質鑒定和定量分析方法,即鳥槍法。該方法可以對樣品同時進行鑒定以及定量研究。被選出的肽段如圖1A中所示,經過串聯質譜儀進行離子掃描分析。在這里,母離子是被隨機選出的,通常母離子的裂解片段中只有一個片段能夠被檢測到,也就是說存在采樣不足的問題。MS1質譜儀采集到的離子強度信息與參考分子信息比對可以進行定量分析,這里使用的參考分子通常都會標記上穩定的同位素標簽。C:定量研究方法能去除蛋白質定量研究與鑒定過程中的干擾信號。首先,MS1質譜儀會通過比對不同樣品的肽模式,即肽段分子量相對色譜保留時間作圖的結果,挑選出不同樣品間豐度不同的肽段。然后被挑出的肽段進入下一輪MS/MS質譜檢測。D:基于各種假說的檢測方法。該方法可以對各種預先被設定肽段的豐度進行高精度的檢測,我們通常都是根據以往的實驗結果來挑選這些靶肽段。在這里常用的方法是圖1D中所示的MRM方法。如果在試驗中選用合適的參考肽段會進一步提高實驗的準確性。
比較模式分析
圖2C中所示的比較模式分析法其實在原理上與2維電泳方法是相似的,就像在2維電泳中一樣,每一個蛋白質都是一個獨立的點,可以借此對它們進行定量和定性的分析。而且還可以進一步對蛋白質進行分析,比如進行蛋白質測序或進行翻譯后修飾情況鑒定等。不過在以質譜檢測手段為基礎的分析方法中,蛋白質樣品首先需要被降解、片段化,然后再用液相色譜-質譜儀LC/MS進行分析。借助色譜洗脫時間和分子量這兩個參數,我們就可以鑒定出一個多肽離子。將所有離子的數量信息整合起來就得到了蛋白質的定量信息。這種方法主要的優勢在于它可以對質譜儀發現的所有信息進行定量處理。與“鳥槍法”相比這是非常明顯的優勢,因為在“鳥槍法”里,只能對被鑒定出來的肽段進行定量化處理。不過在實際運用過程中,這種比較模式分析方法的重復性很差,也沒有非常好的配套軟件對檢測結果進行分析。用這種方法可以獲得一些數據,根據這些數據能夠推測出蛋白質序列,這些數據包括質荷比(m/z)、帶電荷狀態、洗脫時間以及離子強度等。需要被測序的多肽(比如在兩個樣品中表達豐度不同的同一蛋白質)會出現在檢測結果列表中,然后,我們會將該蛋白(多肽)進行新一輪的直接質譜檢測,專門只采集它的MS/MS質譜圖信息。這種研究方法也可用于MALDI/MS/MS質譜檢測平臺,因為蛋白質樣品都被“固定”在樣品板上,因此可以對它們進行不受時間限制的連續檢測。
基于各種假說的研究策略
隨著各種質譜儀技術的不斷進步,我們有理由相信會出現敏感度更高、處理速度更快、更可靠的蛋白質組研究設備。不過目前我們還不清楚這些技術上的進步是否足以突破當下蛋白質組學研究工作中的瓶頸。以前我們曾認為蛋白質組學研究策略需要進行有效的變革才能全面、有力的對蛋白質組進行研究和分析。這種變革的核心就是改變以往那種在每一次試驗中都對既往結果進行重復研究的蛋白質組學研究方法,新的研究策略是根據既往的研究成果來設計、指導進行新的實驗研究項目。我們預計與人類基因組計劃一樣,將來也會獲得某個物種的完整蛋白質組序列圖譜,未來蛋白質組的研究目標應該是對蛋白質(多肽)進行具有特定目的的、非冗余的分析研究。對于質譜技術和質譜儀器的發展來說,這種研究策略的轉變需要有更好的檢測設備和檢測手段(流程)做依托,要能夠以更快的速度、更高的靈敏度和更強大的分析能力進行質譜檢測。現在也出現了可供序列組裝、修飾情況查詢的數據庫。可以預計,在不久的將來,各種生物學假說將會給我們設定出許多待檢測的蛋白質靶標。我們可以將這些蛋白質的信息錄入數據庫,構成一個檢測這些假說所必需的極小集蛋白質信息簇。然后,可以用各種方法,比如MRM方法對這些蛋白質進行檢測(圖2D)。因為這種研究方法主要是對非冗余靶標進行質譜檢測,所以,在檢測的敏感度方面和樣品處理能力方面都有很大的提高。如果再配合定量的、標準化的同位素標記參考肽段,還可以進行精確的定量分析。
上述這種研究策略最適合用于Q-Q-LIT質譜儀這類被我們使用了幾十年,主要用于檢測小分子藥品和體內藥物代謝研究領域的三重四級桿質譜儀。在研究藥物代謝時使用的研究方法同樣適用于蛋白質組學研究領域。
作為上述方法的一個補充,Smith又開發出另一種使用精確分子量標簽來鑒定蛋白質的方法。該方法首先測定待測物質的分子量,然后將數據與分子量數據庫進行比對,以此來鑒定蛋白質。這樣就無需再對每一個樣品中的每一條多肽進行測序了。隨著蛋白質組學研究的不斷開展,我們積累的數據也越來越多,并且數據積累的速度也越來越快,同時,各種分析軟件的功能也越來越強大,因此我們相信,基于各種假說的蛋白質組學研究策略一定會被更多的人所接受,所采用。
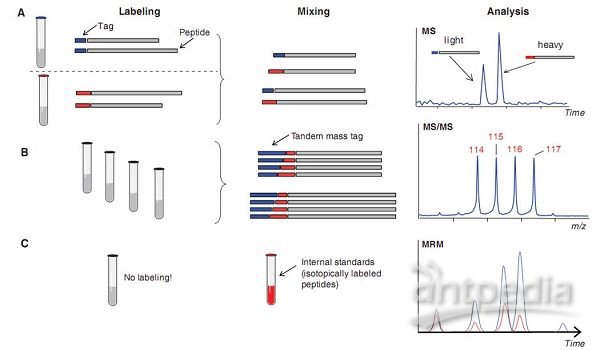 肽段定量分析策略示意圖
肽段定量分析策略示意圖
Labeling:標記 Tag:標記物 Peptide:肽段 Mixing:混合 Analysis:分析
MS:質譜檢測 light:較輕的片段 heavy:較重的片段 Time:時間
Tandem mass tag:串聯標簽 MS/MS:MS/MS模式 m/z:質荷比
No labeling!:為標記 MRM:MRM方法
Internal standards(isotopically labeled peptides):內參,即同位素標記的肽段
圖3 肽段定量分析策略示意圖。A:同位素稀釋法是進行肽段定量分析時最常用的一種方法,該方法也是進行蛋白質組學研究時常用的一個方法。該方法的原理是在一號樣品所有的待測蛋白質上都帶上一個穩定的同位素標簽,同時在二號樣品所有的待測蛋白質上都帶上另一個穩定的同位素標簽。這樣,這兩組樣品就可以互為參照了。可以借助化學的方法,例如穩定的同位素編碼標簽試劑、代謝標記反應和酶標反應等對蛋白質進行同位素標記。B:使用串聯標簽進行定量研究。該方法同樣需要各種穩定的同位素標記物。這些同位素標記物由兩種同位素標記元素組成,它們都有固定的分子量。目前,這些試劑可用于四通道反應。通過在質譜儀的MS/MS模式下檢測連接在蛋白質N端報告基團的相對強度以及CID圖譜中低分子量范圍里的信號可以獲得待測蛋白質的定量信息。C:使用內參進行定量研究的方法。該方法實際上也是一種同位素稀釋法。在該方法中會往待測樣品中添加一種已知濃度的同位素標記的肽段,然后借助標準曲線進行精確的定量分析。雖然該方法樣品制備過程較為復雜,但是它的前景非常光明。它非常適合用于基于各種假說的檢測方法。
結論與展望
在過去的十年里,是蛋白質分析,更準確的說應該是蛋白質組學分析推動了質譜檢測技術的發展。各種技術進步已經使質譜儀在準確度、分辨力、敏感度、定量分析能力等各方面都有了長足的進展,蛋白質組質譜檢測策略方面也有了新突破。分析完整蛋白質、蛋白質復合體、低豐度蛋白質等各種樣品的檢測操作流程層出不窮。雖然這些質譜檢測技術是為了滿足蛋白質分析的需求而誕生的,但是它們出現之后又反過來推動了生物大分子(包括代謝產物、脂類物質、碳水化合物等等)領域的研究。因此,我們有理由相信,質譜檢測技術必將在生物研究的各個領域里占有重要的一席之地。
公告內容為便于供應商及時了解政府采購信息,根據《財政部關于開展政府采購意向公開工作的通知》(財庫〔2020〕10號)等有關規定,現將本單位2025年10月至2025年11月采購意向公開如下:序號采購項......
zycgr220119012025年10至12月政府采購意向-脂質分析質譜系統詳細情況脂質分析質譜系統項目所在采購意向:zycgr220119012025年10至12月政府采購意向采購單位:zycgr......
項目概況中國政法大學 證據科學研究院進口設備采購項目招標項目的潛在投標人應在北京明德致信咨詢有限公司 官網(http://www.zbbmcc.com)獲取招標文件,并于2025年......
政府采購意向公告廣東石油化工學院 2025年10月至2025年11月政府采購意向為便于供應商及時了解政府采購信息,根據《財政部關于開展政府采購意向公開工作的通知》(財庫〔2020〕10號)等......
為便于供應商及時了解政府采購信息,根據《財政部關于開展政府采購意向公開工作的通知》(財庫〔2020〕10號)等有關規定,現將青海師范大學(本級)2025年度(第28批)采購意向公開如下:序號采購項目名......
為便于供應商及時了解政府采購信息,根據《財政部關于開展政府采購意向公開工作的通知》(財庫〔2020〕10號)等有關規定,現將安徽農業大學2025年10月采購意向公開如下:序號采購項目名稱采購需求概況預......
中南大學 2025年11月政府采購意向公開為便于供應商及時了解政府采購信息,根據《財政部關于開展政府采購意向公開工作的通知》(財庫〔2020〕10號)等有關規定,現將中南大學2025年11月......
中南大學 2025年11月政府采購意向公開為便于供應商及時了解政府采購信息,根據《財政部關于開展政府采購意向公開工作的通知》(財庫〔2020〕10號)等有關規定,現將中南大學2025年11月......
一、項目編號421301202501000321二、采購計劃備案號隨采計備[2025]00587號三、項目名稱超高效液相色譜串聯質譜檢測系統、高通量基因測序儀四、中標(成交)信息供應商名稱:華潤隨州醫......
為便于供應商及時了解政府采購信息,根據《財政部關于開展政府采購意向公開工作的通知》(財庫〔2020〕10號)等有關規定,現將西華大學2025年度(第30批)采購意向公開如下:序號采購項目名稱采購需求概......