1.鄰近定向 對一個雙分子反應,酶可以使兩個底物結合在活性中心彼此靠近,并具有正確的取向。這比在溶液中隨機碰撞更容易發生反應。鄰近效應相當于大大提高了有效底物濃度,甚至超過現實中可以達到的濃度。定向效應則使每一次碰撞都具有正確的取向。化學上通過將分子間反應轉變成分子內反應對此進行推算,認為可以將反應速度加快100倍到10的11次方倍。
2.底物形變 酶與底物結合時,誘導契合現象不僅酶的構象發生改變,底物的構象也會發生變化。這種變化使底物更接近于過渡態,因此可以降低活化能。例如,N-乙酰胞壁酸的糖環正常情況下是椅式構象,但與溶菌酶活性中心結合后,會被誘導變成半椅式構象,從而使其糖苷鍵更容易斷裂。
溶菌酶誘導底物構象改變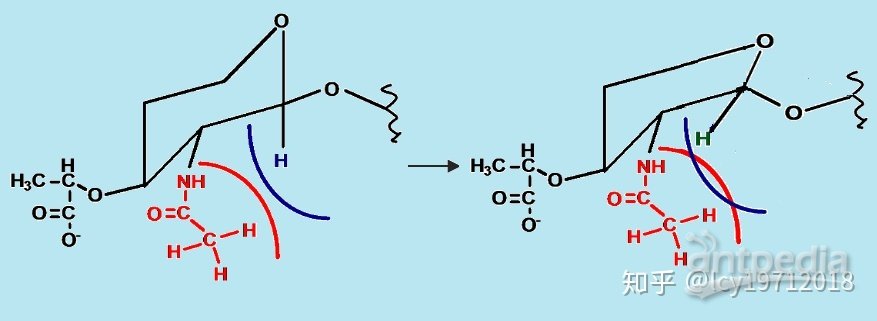
3.微環境 酶的活性中心是一個相對封閉的空間,其性質與溶液中有所不同,所以稱為微環境。例如,有些酶的活性中心是一個疏水的微環境,其介電常數較低,有利于電荷之間的作用,也有利于中間物的生成和穩定。賴氨酸側鏈氨基的pK約為9,而在乙酰乙酸脫羧酶活性中心的賴氨酸側鏈pK只有6左右。這也是某些專一性抑制劑只與酶活性中心的基團反應的原因。
4.直接催化 酶分子中含有不同化學特性的基團,如殘基的側鏈基團、金屬離子以及輔酶輔基等。其中某些基團可以直接與底物作用,或者通過穩定過渡態來降低活化能,或者通過改變反應進程繞過高活化能的反應步驟。酶的直接催化作用可以分為酸堿催化、共價催化和金屬離子催化。
共價催化通過生成共價中間體穩定過渡態,經常形成反應活性很高的共價中間物,將一步反應變成兩步或多步反應,繞過較高的能壘,使反應快速進行。例如胰蛋白酶通過絲氨酸側鏈羥基形成酰基絲氨酸共價中間物,降低活化能。而賴氨酸的氨基經常生成西弗堿共價中間物。
西弗堿反應
共價催化可分為親電催化和親核催化。羥基、巰基和咪唑基都有親核催化作用。絲氨酸蛋白酶、含巰基的木瓜蛋白酶、以硫胺素為輔酶的丙酮酸脫羧酶都有親核催化作用。氫離子、金屬離子、-NH3+、磷酸吡哆醛等是親電基團,例如轉氨酶就是通過親電機制催化的。