IVIg凍融制劑的加速應力試驗
用含1mg /mL IVIg的4ml配方填充硼硅酸鹽瓶(6ml)和SiOPlas?瓶(6ml), PBS pH
7.4。小瓶的內容物經過1或6次凍融循環。在每個凍融循環中,小瓶先在液氮中浸泡2 min,然后在30_C水浴中解凍14.5
min,輕輕旋轉攪拌后再進行下一個凍融循環。
亞可見粒子濃度分析
如前所述,使用流式成像顆粒分析儀(FlowCAM?,Fluid imaging Technologies, Scarborough, ME)獲取不同強調配方中的顆粒濃度和顆粒圖像。經過6次凍融循環的樣品中顆粒濃度接近或超過流動成像顯微鏡儀器的上限,因此在分析前用pH
7.4的PBS稀釋100倍。在強調的配方中,顆粒計數被測量在相同的單個注射器和小瓶被測試補體激活的樣本中。每個樣品都有一個顆粒大小分布;在測試強化配方激活補體的能力之前,盡量不讓顆粒分形。
表1 進行補體激活試驗的受應力樣品中亞可見顆粒的濃度
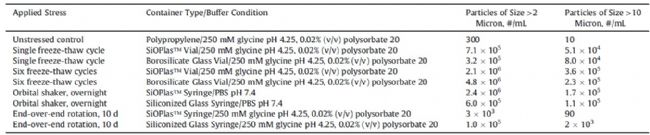
從每個應力/容器組合中收集3個樣品。容器與容器之間的顆粒濃度差別<15%。
可溶性蛋白組分的排阻色譜分析
排阻色譜被用來監測單體蛋白的保留和在應用攪拌或凍融應力后IVIg樣品中任何可溶性聚集物的外觀。TSKgel G3000SWXL柱(TOSOH
Biosciences, montgomery yville PA)與Agilent 1100系列柱(Santa Clara,
CA)一起使用。洗脫液在安捷倫化學站軟件中以280 nm的吸光度進行監測。流動相為100mm硫酸鈉、100mm磷酸鈉和pH為6.7的0.05%
(w/v)疊氮化鈉,以0.6 mL/ min的速度通過系統。色譜圖中的峰面積用GRAMS/AI version 9.1 (Thermo
Fisher Scientific Inc., Waltham,
MA)進行量化。在應用加速應力條件后,從(本質上)無顆粒、離心和過濾的起始配方的可溶性蛋白的部分損失被量化使用峰面積的比率為應力和非應力配方。
人類血清樣本中的補體激活
從3個小瓶或注射器中收集的不同應激IVIg制劑的樣品以及每種制劑的非應激對照樣品被送往Exsera BioLabs (Denver,
CO),以分析它們激活補體的能力。補體激活在3個個體獻血者的正常血清池中進行了測量,這些獻血者之前曾篩查過補體功能正常。將脅迫的IVIg制劑的試驗樣品稀釋10倍到混合的人血清中,混合后在37°C孵育30分鐘。孵育后,樣品在80°C保存,直到進行進一步的測試。為了分析補體的活化,使用從Quidel公司(San
Diego,
CA)購買的試劑盒,采用ELISA法測定了四種補體級聯活化片段C3a、Bb、C4a和C5a的濃度。選擇C4a是因為它是經典或凝集素通路激活的標志,Bb是補體激活備選通路的明顯標志,C3a是補體激活的中心點,C5a是補體通路終端激活的標志。對四種補體級聯蛋白分別進行了40次3遍重復ELISA檢測。除了測試應激IVIg樣本,還分析了幾個對照。這些對照樣品僅包含混合血清或血清樣品,其中以1:9的比例加入含zymosan的生理鹽水PBS或含熱聚集伽馬球蛋白的PBS。測量的平均值與顆粒樣本計數相比,在鹽水對照中測量的濃度增加了一倍。
結果
IVIg配方的加速應力測試中顆粒的形成
正如預期的那樣,每種加速應力測試方法都會在測試配方中產生微顆粒(表1)。在pH 7.4的PBS條件下,IVIg的凍融產生的亞可見顆粒最多。在硼硅酸鹽和SiOPlas?瓶中,一次凍融循環分別產生3.2?105和7.1?105個粒徑大于2微米的顆粒。也生產了大于10微米的顆粒,在硼硅酸鹽瓶中檢測到8.0?104個顆粒,在SiOPlas?瓶中檢測到5.1?104個顆粒。
多次凍融循環使顆粒數進一步增加了約一個數量級(表1)。6次循環后,硼硅酸鹽瓶和SiOPlas?瓶中的顆粒濃度分別增加到:大于2微米的4.8?106和2.1?106個顆粒/mL。也生成了大于10微米的顆粒,分別在硼硅酸鹽瓶和SiOPlas?瓶中生成2.3?105和3.6 ?105個顆粒。
由于攪拌應力而產生的顆粒數量取決于容器類型和所應用的攪拌類型。使用定軌搖床pH值7.4 PBS中的IVIg配方進行晝夜不間斷攪拌,在硅化玻璃注射器中產生了大于2微米的顆粒濃度6.0?105個/毫升,以及在SiOPlas?注射器中產生了2.4?106個顆粒 /毫升,如 (表1)。與凍融研究一樣,兩種類型的注射器形成大顆粒(> 10微米) 的差別約一個數量級。
在“端到端”旋轉10天的加速穩定性試驗中。pH為4.25甘氨酸IVIg制劑在硅化玻璃注射器和SiOPlas?注射器中分別檢測到粒徑大于2微米的1.0?105和3?103顆粒/mL。相應的,大于10微米的顆粒也較少,在硅化玻璃和SiOPlas?注射器中分別檢測到2.0? 103和90個顆粒/mL。
圖1展示了由各種加速應力方法產生的典型的由流式顆粒成像分析儀(FlowCam)所捕捉到的顆粒圖像。在小瓶中,凍融應力下的樣品主要含有具有蛋白質聚集物特征的非球形微粒,硅化玻璃注射器中攪拌應力下的樣品包含大量球形顆粒,這是滴潤滑劑顆粒的特點(圖1
a、c、e和f)。在SiOPlas?注射器中,攪拌應力作用下產生顆粒具備形狀不規則蛋白質聚體和球形硅油液滴(圖1 b和d)。
對于所有的加速應力條件測試,尺寸排除色譜分析顯示,只有<5%的不溶性蛋白形成。在任何條件下均未檢測到可溶性聚集物。在硼硅玻璃小瓶中,6次凍融循環使IVIg產生的顆粒濃度最高,達到大于2微米顆粒500萬個/毫升,但這僅表示損失了3.7%的原始單體蛋白。
在加速應激條件下產生的顆粒對人血清中的補體激活
當IVIg配方被稀釋10倍于人血清時,在加速應激條件下,IVIg配方中大于2微米的顆粒與激活補體呈線性關系(圖2-4)。在大于10微米顆粒數量較多的樣本中,補體激活水平通常較高,但這些較大顆粒的水平較低,不能明確的劑量的相關性見圖5。
觀察到的補體激活與通過替代途徑的激活一致。沒有增加C4a鹽水控制水平,這是一個典型的標志或凝集素途徑(圖6)。相比之下,Bb,補體激活的標記的替代途徑,增加線性(r2=0.94)的濃度大于2微米粒子尺寸范圍的增加(圖2)。
增加過敏毒素的濃度C3a Ca5也觀察到當粒子被稀釋到血清(圖3和4)。與Bb響應,褶皺增加與鹽水控制線性依賴于粒子的劑量,與相關系數r2
C3a和ca5的0.85和0.99,分別。對IVIg配方的反應,在硼硅酸鹽玻璃小瓶中經過6次凍融循環后,C3a和C5a的濃度增加了2.4-
8.9倍,比在生理鹽水對照組中觀察到的要高。