近日,以封面形式發表在《Science Translational Medicine》上的一篇研究中,來自美國冷泉港實驗室(CSHL)的研究人員已經確定了10種目前正在進行臨床試驗的癌癥藥物并未靶向目標蛋白,因此藥物不能按預期發揮作用。
這一發現緣于一個完全不同的事件。在過去的幾年里,CSHL的研究員Jason Sheltzer的實驗室一直致力于識別與癌癥患者低生存率相關的基因。在這項研究中,研究人員發現母體胚胎亮氨酸拉鏈激酶(Melk,一種經常在腫瘤中發現的高水平蛋白質),對癌癥的生長完全沒有影響。

Jason Sheltzer 圖片來源:CSHL
這一結果令人震驚,因為此前已有數十篇學術論文將MELK確定為一種癌癥“成癮”所需的蛋白質,對癌細胞的存活至關重要。然而,當Sheltzer團隊使用CRISPR介導的基因編輯來消除MELK,發現癌細胞并沒有任何可檢測的損失。
Sheltzer說:“這令我們大為驚訝,癌細胞沒有死亡。它們并不依賴MELK。”
經過反復的嚴格檢查,Sheltzer實驗室不得不得出結論,Melk并不是被吹捧的理想癌癥藥物靶點。
當時,Sheltzer和他的同事警告研究人員和醫學界,這可能是一個普遍性的問題,會導致許多有前景的癌癥藥物被錯誤描述。但為了證實他們的懷疑,研究團隊不得不進行更多的測試。
Sheltzer說:“我的目的是調查MELK是否存在異常,但我發現事實并非如此。”
在這篇新論文中,Sheltzer與Chris Giuliano領導的一個研究團隊詳細描述了10種藥物的“作用機制”是如何被曲解的,就像MELK一樣。
Sheltzer解釋道:“這些藥物被設計用來阻斷癌細胞中某種蛋白質的功能。我們所展示的是,大多數這些藥物并不是通過阻斷蛋白質功能來發揮作用的。這就是所謂的作用機制。”
所有10種藥物目前都在臨床試驗中進行測試,涉及大約1000名人類癌癥患者。雖然它們確實有殺死癌細胞的能力,但并不像研究人員想象的那樣。
Sheltzer說:“從某種意義上說,這是我們所面臨的新一代技術問題”。
在CRISPR基因編輯之前,大多數科學家用來干擾特定蛋白質產生的技術被稱為RNA干擾(RNAi)。該方法允許研究人員防止細胞讀取由任何一種基因產生蛋白質的指令。但與CRISPR不同的是,RNAi技術只能進行干擾,而CRISPR可以完全破壞或移除特定基因。這一過程也有可能潛在干擾人體細胞中其他已知蛋白質的產生。
這正是Sheltzer及其同事所懷疑的,不僅MELK發生了這種情況,而且其他六種有希望的蛋白質也發生了同樣情況,它們并不是癌細胞生長所必需的。更有趣的是,當研究團隊利用靶向這些蛋白的藥物處理缺乏該蛋白的癌細胞時,癌細胞還是死亡了。這表明,這些藥物顯然是通過其他機制來發揮抗癌作用的。
為此,他們選擇了10種藥物中的一種,這是一種通過抑制蛋白質PBK殺死癌細胞的藥物。但是Sheltzer發現它在做著一些非常不同的事情。
Sheltzer說:“研究結果表明,PBK與癌細胞的這種相互作用與它如何殺死癌細胞沒有任何關系。”
為了找出真正的抗癌作用機制,他的團隊將癌細胞暴露在“濃度非常非常高”的PBK靶向藥物中。然后,他們給這些細胞足夠的時間來產生耐藥性。
Sheltzer說:“癌癥在基因組中高度不穩定。由于這種固有的不穩定性,培養皿中的每個癌細胞都與其旁邊的不同。隨機獲得阻斷藥物有效性基因改變的癌細胞將會成功,而其他的則會被殺死。我們可以利用這一點。另外,通過識別這種基因變化,我們還可以確定這種藥物是如何殺死癌細胞的。”
研究團隊發現,癌細胞通過突變產生的蛋白質CDK11基因進化出抗藥性。該基因突變的方式使藥物不再與其相互作用,就像生銹的鐵門再也不能用鑰匙鎖住一樣。
與其他一些驗證性實驗一起,這些結果告訴研究團隊CDK11是對抗癌癥的真正作用機制。有了這些知識,研究人員現在希望設計出更好的藥物,更具體地靶向CDK11。
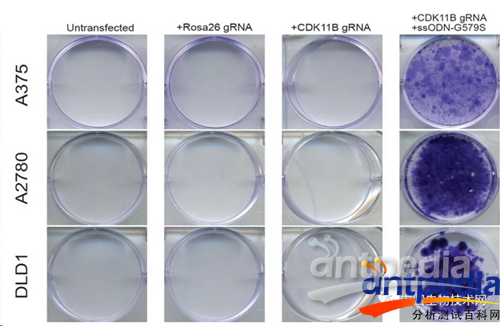
研究人員將各種突變的癌細胞暴露于致癌藥物OTS964中,幾乎所有的菌株(第1-3列)都被殺死。只有當它們突變以抵抗藥物阻斷其CDK11蛋白受體的能力時,癌細胞才會繁殖(染成紫色),這表明CDK11對于癌癥生長或癌癥“成癮”至關重要。圖片來源:Sheltzer lab / CSHL
Sheltzer說:“很不幸,許多在人類癌癥患者中進行測試的藥物最終并沒有幫助到他們。如果在藥物進入臨床試驗前定期收集這類證據,我們可能會更好地將患者分配最有可能為其帶來益處的療法。憑借這些知識,我相信我們可以更好地實現精準醫學。”
科技日報訊(記者張佳欣)美國西奈山伊坎醫學院研究人員開展的一項新研究,探索了衰老免疫系統是如何促進腫瘤生長的,為癌癥預防和治療提供了新見解。相關論文發表在近期《科學》雜志上。黃色和藍色分別表示表達IL......
鐵死亡是一種鐵依賴性的、非凋亡性、程序性細胞死亡,因其獨特的機制在腫瘤治療和神經退行性疾病領域引起廣泛關注。近日,中國科學院杭州醫學研究所(以下簡稱杭州醫學所)研究員覃江江課題組、程向東教授團隊聯合研......
鐵死亡是一種鐵依賴性的、非凋亡性、程序性細胞死亡,因其獨特的機制在腫瘤治療和神經退行性疾病領域引起廣泛關注。近日,中國科學院杭州醫學研究所(以下簡稱杭州醫學所)研究員覃江江課題組、程向東教授團隊聯合研......
論文標題:RepurposedbenzydaminetargetingCDK2suppressesthegrowthofesophagealsquamouscellcarcinoma期刊:Fronti......
中新網北京8月27日電(記者孫自法)施普林格·自然旗下專業學術期刊《自然-心血管研究》最新發表一篇生物學論文稱,研究表明,常用于治療多發性硬化癥的藥物醋酸格拉替雷(Glatiramer-acetate......
近日,國際學術期刊《自然-通訊》(NatureCommunications)在線發表研究論文:來自美國猶他大學的科研人員在致命的芋螺(雞心螺)毒液中發現了一種新毒素,其特殊而持久的作用有望幫助科學家設......
中國科學院上海藥物研究所研究員刁星星課題組、陳浩課題組,運用放射性標記技術,成功合成[14C]ARV-110作為PROTAC(蛋白水解靶向嵌合體)的代表性模型化合物,并揭示了PROTAC在口服生物利用......
·“未來的干細胞產品主要產生在兩個方向上,一是慢性病治療,比如心衰、帕金森病、漸凍癥等,二是抗衰老相關產品,比如面膜、化妝品、吸入式抗衰老產品等。”“產品是第一位的,如果沒有產品,其他所有的基礎設施和......
根據中國藥品監督管理局官方網站數據,小編整理了2024年上半年新注冊的臨床質譜相關產品共31項,其中質譜儀器11項,檢測試劑、試劑盒18項,標準品、質控品2項。其中2臺獲批質譜儀器為進口產品,其余均為......
近年來,將藥物和功能細胞進行偶聯成為一種新興藥物形態。日前,浙江大學藥學院、金華研究院教授顧臻和研究員王金強等在《自然·生物醫學工程》上發表綜述論文,將這類形態的藥物定義為細胞偶聯藥物。論文總結了細胞......