我們的身體能夠感知多種機械刺激,我們的觸覺能夠有效區分微風吹過皮膚的感覺和引發疼痛的按壓感。Piezo1和Piezo2離子通道能夠通過允許正離子在細胞膜表面流動來響應細胞膜上的力,從而介導動物機體中多種機械刺激過程。這種機械性的電轉導由感覺神經元中的Piezo2以及非神經元中的Piezo1所介導,其能對諸如剪切力和滲透力等驅動力作出反應。
圖片來自Nature, doi:10.1038/s41586-019-1505-8。
Piezo離子通道由三個相同的Piezo蛋白所組成,每個蛋白都含有2500個氨基酸殘基,解析如此龐大的結構并找到每個原子的位置是一項非常大的挑戰,盡管如此,在過去幾年里,人們已經在近原子分辨率下描述了Piezo1的部分結構。
此外,包括巨噬細胞和單核細胞在內的免疫系統骨髓細胞會暴露于一系列物理壓力中,比如當其離開血管進入組織后就會遭遇這些物理壓力,機械力的周期會發生在諸如肺部等器官中,在呼吸過程中這些組織就會被壓縮,這些力量本身也會在疾病狀態下發生改變。
近期,Nature期刊在同一天發表三篇關于Piezo2和Piezo1的論文,其中的第一篇論文涉及解析Piezo2的三維結構,第二篇涉及解析Piezo1的三維結構,第三篇論文闡明巨噬細胞和單核細胞能對機械線索產生反應,而這些反應是通過位于細胞表面的稱之為PIEZO1的機械感應離子通道所感知的。
在第一項發表在Nature期刊上的研究中,Wang等人進一步研究了Piezo2的近原子分辨率結構,并解析了38個跨膜螺旋,這是單顆粒低溫電子顯微鏡(cryo-EM)“分辨率革命”的又一成就,cryo-EM能通過分析數千個單個蛋白的分子圖像來獲得分子結構,這些蛋白分子能被隨機凍結在一層薄薄的非晶冰中。實踐證明,cryo-EM能夠解析大型膜蛋白(比如離子通道)的結構,而利用X射線晶體學技術無法直接或許這些膜蛋白的結構。

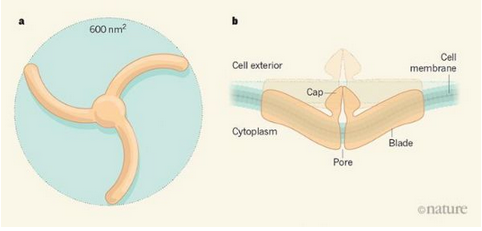
Wang等人利用此前報道的Piezo1的結構作為Piezo2的模型,由此所產生的Piezo2的巨大結構或許就是多個實驗室多年研究的結晶。這些研究結果表明,Piezo通道有四個關鍵特征,研究者給予這些特征進行了描述,即螺旋槳(propeller),帽(cap),孔(pore)和納米碗(nano-bowl)(有時也稱為圓頂);螺旋槳結構有三個葉片,每個葉片都由一個組成蛋白質組成,其圍繞中心均勻分布,每個葉片的長度為200埃分辨率,而且每個葉片包含36個α螺旋,其擁有穿過脂質雙層的正確長度,并能疏水性地嵌入其中。因此,螺旋串可能會在膜上來回“編織”,三個類似彈簧的刀片結構共同限定了約600平方納米的膜區域,其能用于膜拉伸傳感器的聲音布置。
帽結構則位于孔外較大的細胞外結構域中,其類似于參與其它三聚體離子通道的門控相關的帽狀結構,孔區域由6個α螺旋組成,其擁有允許正離子通過的內表面電荷,Piezo1和Piezo2的孔隙能在被解析的結構中夾緊,Piezo1中有一個收縮部位,而Piezo2中則有兩個收縮部位。
在第二項發表在Nature期刊上的研究中,Lin等人對脂質囊泡中的Piezo1進行了研究,這非常重要,因為此前報道的Piezo結構是在洗滌劑的聚集體中獲得的,而并非在脂質中,所以人們并不清楚Piezos如何坐落到脂質雙層中并與之相互作用。Lin等人指出,Piezo1確實會將囊泡折疊成為非球形結構。此外,Lin等人使用原子力顯微鏡(AFM)探針對Piezo通道施加外力,結果發現,碗狀結構在生物壓力下發生了可逆的變平效應。

值得注意的是,AFM垂直于對膜所施加的力量,而并不是橫向穿越膜,但實驗結果仍然證實了碗狀結構在適當外力下的彈性,然而,該實驗并未解決是否生物性的刺激能夠直接拉伸細胞膜或通過輔助的蛋白來發揮作用。同樣研究者也并不清楚碗狀結構的扁平化如何打開孔狀結構,細胞外帽結構或許對于孔狀結構的開啟非常重要,正如Wang等人所說的那樣,消除大部分突變能夠使得通道對膜的變形不再敏感,然而,當大部分蛋白被剔除時,或許就有許多方法能夠解釋蛋白功能的喪失了。
在第三項發表在Nature期刊上的研究中,Solis等人通過研究揭示,小鼠肺部產生的機械線索或能被免疫細胞所感知,而且其是對于免疫反應最重要的調節因素,此外,巨噬細胞和單核細胞能對機械線索產生的反應是通過位于細胞表面的稱之為PIEZO1的機械感應離子通道所感知的。

為了理解骨髓細胞暴露于機械力是否能夠直接調節免疫細胞的功能,Solis等人培育出骨髓細胞缺少PIEZO1的基因工程小鼠,利用體外系統,他們讓小鼠機體的免疫系統處于壓力改變的循環中,這樣就能夠模擬肺部遭遇的損傷,稱之為周期性靜水壓力(cyclical hydrostatic pressure)。他們隨后比較了野生型和缺失PIEZO1的巨噬細胞和和單核細胞,結果表明在依賴于PIEZO1的野生型細胞中,周期性靜水壓力能誘導促炎性基因表達譜,包括受到轉錄因子HIF1α控制的基因,其中HIF1α是基因表達的關鍵調節因子,也是是髓系細胞維持功能和生存所必需的。更有意思的是,這種促炎性基因表達并不會受壓力大小的影響。
為了理解驅動這種轉錄反應的分子機制,Solis等人對缺失HIF1α的巨噬細胞進行了研究,他們發現,細胞無法應對周期性靜水壓力導致的促炎性基因表達反應。在體外系統中,讓野生型細胞遭受這類壓力會驅動鈣離子通過PIEZO1通道流入細胞,從而導致HIF1α積累,PIEZO1所介導的HIF1α水平增加需要產生內皮素1。內皮素1能夠在一種穩定細胞中HIF1α的信號通路起作用。內皮素1能被細胞分泌,并通過結合在細胞表面上的受體或附近細胞上的受體來發揮作用。
為了檢測PIEZO1介導的信號在宿主防御中扮演的關鍵角色,Solis等人利用被銅綠假單胞菌感染引起肺炎的小鼠模型進行研究,與野生型小鼠相比,骨髓細胞中缺少PIEZO1的小鼠肺部組織中中性粒細胞的水平較低,而且肺部組織中促炎性免疫信號分子的水平較低,比如內皮素1;同時這類小鼠機體中CXCL2的水平也較低,CXCL2能夠吸引中性粒細胞;相比野生型小鼠而言,這類小鼠肺部中的細菌水平更高,而且擴散到肝臟中的細菌水平也較高。
如果在肺泡的巨噬細胞中剔除PIEZO1,或在樹突細胞中剔除這種離子通道的話,小鼠機體中內皮素1的產生并不會受到影響;然而,剔除單核細胞則會導致內皮素1的水平下降,這就提示這類細胞或許是內皮素1的來源。Solis等人證實,PIEZO1依賴性的內皮素1產生在機體抵御感染的防御上扮演著非常關鍵的角色,與未注射內皮素1的小鼠相比,給缺少PIEZO1的小鼠機體的骨髓細胞注射內皮素1能夠降低有害細菌的負擔。這些研究結果與對另外一種模型的研究結果一致,即PIEZO1所介導的肺部組織單核細胞的機械感應激活這些細胞產生內皮素1,從而促進HIF1α水平上升和促炎性基因表達,從而招募中性粒細胞來幫助抵抗有害細菌入侵。
2025年,科學領域將迎來一系列備受矚目的突破與挑戰,從新一代抗肥胖藥物的問世,到改變未來的太空探索任務,再到關乎全球氣候政策的關鍵會議,這些發展不僅影響著科學研究的前沿,也與每個人的生活息息相關。近......
近日,國際頂級科學雜志《自然》在線發布了中國科學家領銜發起、十八位兩院院士和十八國科學家團隊聯合署名的人體蛋白質組導航國際大科學計劃(ProteomicNavigatoroftheHumanBody,......
冠狀病毒已經在本世紀引發了三次重大疾病爆發,包括COVID-19大流行,科學家們懷疑潛伏在自然界中的其他家族成員威脅著人類。但是,這些病原體中的許多都很難在實驗室中生長,這使得在它們襲擊之前研究它們并......
能夠在CNS(Cell、Nature和Science)等國際頂尖學術期刊上發表論文,對于科研人員可以說是夢寐以求的,其實,早在140年前的清朝末期,中國人就在Nature上發表了第一篇論文——《考證律......
中國學者關于CAR-T細胞療法的研究登上Nature(自然)官網頭條。10月5日Nature官網首頁,頭條文章關注中國學者發表的國際首個通用CAR-T治療自身免疫病成果。網站截圖10月5日,澎湃新聞記......
近日,北京科技大學新金屬材料國家重點實驗室呂昭平教授團隊一月內在《NatureCommunications》連續發表兩篇論文。呂昭平教授團隊研究成果介紹01高熵非晶合金中的連續多形性轉變非晶態多形性轉......
從27歲成為臺積電的基層工程師,到32歲成為最年輕的項目主管經理,再到35歲出國做博士后,直至37歲出站后成為香港大學最年長的助理教授,沒有“人才帽子”的馮憲平如今已是香港城市大學工程學院的副院長。就......
近年來偽狂犬、猴痘等病毒從動物向人類外溢引發新發傳染病甚至全球大流行的頻率正在顯著增加如何精準預測和預報動物源新發傳染病是關系綠色健康養殖與公共衛生防控的重要科學問題復旦大學公共衛生學院粟碩教授團隊與......
乙酰膽堿通過廣泛的膽堿能神經支配調節多種認知功能。然而,特定的膽堿能亞群、回路和識別記憶的分子機制在很大程度上仍然未知。2024年8月26日,清華大學魯白及首都醫科大學YangFeng共同通訊在Nat......
文|《中國科學報》記者張晴丹當平常夫妻都在討論柴米油鹽時,上海交通大學副教授李聽昕和劉曉雪這對科研眷侶的畫風卻是這樣的:“實驗為什么會出現這個現象呢?我們一起研究一下。”學術圈里的“夫妻檔”很常見,但......